开尔文方程
编辑开尔文方法描述了由于弯曲的液体-蒸汽界面(例如液滴表面)引起的蒸汽压变化。 凸曲面处的蒸气压高于平面处的蒸气压。 开尔文方法依赖于热力学原理,并不暗示材料的特殊性质。 它还用于使用吸附孔隙度法测定多孔介质的孔径分布。
配方
编辑这可以写成以下形式,称为 Ostwald–Freundlich 方程:ln p p s a t = 2 γ V m r R T , 其中 p 是实际蒸气压, p s a t 是表面平坦时的饱和蒸汽压, γ 是液体/蒸汽表面张力, V m是液体的摩尔体积,R 是通用气体常数,r 是液滴的半径,T 是温度。
平衡蒸气压取决于液滴大小。
如果蒸汽被冷却,则 T 会减少,但 p s a t 也会减少。 这意味着 p / p s a t 随着液体冷却而增加。 γ和 V m 可以视为近似固定,这意味着临界半径 r 也必须减小。 蒸气过冷得越多,临界半径变得越小。 最终它可以变得像几个分子一样小,并且液体经历均匀的成核和生长。
蒸气压的变化可归因于拉普拉斯压力的变化。 当拉普拉斯压力在液滴中升高时,液滴往往更容易蒸发。
在应用开尔文方法时,必须区分两种情况:一滴液体在其自身蒸气中会导致液面凸起,而液体中的气泡会导致液面凹陷。
使用吉布斯自由能推导
编辑体积 V 、压力 P 和温度 T 的吉布斯自由能的正式定义如下:
G = U + p V − T S ,
其中 U 是内能,S是熵。 吉布斯自由能的微分形式可以表示为
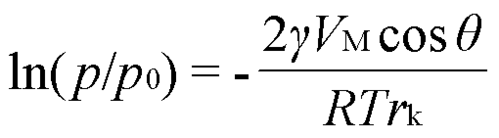
其中 μ 是化学势,n 是摩尔数。 假设我们有一种不含杂质的物质 x 。 让我们考虑一下半径为 r 的单滴 x 的形成,其中包含来自其纯蒸气的 n x 分子。 由于这个过程,吉布斯自由能的变化是
Δ G = G d − G v
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/215186/
