理想气体状态方程
编辑系统属性注意:共轭变量以斜体显示
材料特性
- 属性数据库
可压缩性 β = − {dISPlaystyle beta =-}
热膨胀 α = {diSPlaystyle alpha =}
方程式
- 卡诺定理
- 克劳修斯定理
- 基本关系
- 理想气体状态过程
潜力
- 自由能
- 自由熵
- 内能 U ( S , V ) {displaystyle U(S,V)}
- 焓 H ( S , p ) = U + p V {displaystyle H(S,p)=U+pV}
- 亥姆霍兹自由能 A ( T , V ) = U − T S {displaystyle A(T,V)=U-TS}
- 吉布斯自由能 G ( T , p ) = H − T S {displaystyle G(T,p)=H-TS}
- 历史
- 文化
科学家们
- 伯努利
- 玻尔兹曼
- 布里奇曼
- 卡拉西奥多里
- 卡诺
- 克拉佩龙
- 克劳修斯
- 德唐德
- 迪昂
- 吉布斯
- 冯·亥姆霍兹
- 焦耳
- 刘易斯
- 马修
- 麦克斯韦
- 冯迈耶
- 能斯特
- 昂萨格
- 普朗克
- 兰金
- 史密顿
- 斯塔尔
- 泰特
- 汤普森
- 汤姆逊
- 范德瓦尔斯
- 沃特斯顿
其他
- 成核
- 自组装
- 自组织
- 秩序与混乱
理想气体定律,也称为一般气体方程,是一种假设的理想气体的状态方程。 它是许多气体在许多条件下行为的良好近似,尽管它有一些局限性。 它由 Benoît Paul Émile Clapeyron 于 1834 年首次提出,它是经验波义耳定律、查尔斯定律、阿伏伽德罗定律和盖-吕萨克定律的组合。 理想气体定律通常以经验形式书写:
p V = n R T {displaystyle pV=nRT} 其中 p {displaystyle p} , V {displaystyle V} 和 T {displaystyle T} 是压力、体积和温度; n {displaystyle n} 是物质的数量; 并且 R {displaystyle R} 是理想气体常数。它也可以从微观动力学理论推导出来,正如奥古斯特·克伦尼希 (August Krönig) 于 1856 年和鲁道夫·克劳修斯 (Rudolf Clausius) 于 1857 年所取得的(显然是独立地)。
方程式
编辑一定量气体的状态由其压力、体积和温度决定。 等式的现代形式将这些简单地以两种主要形式联系起来。 状态方程中使用的温度是绝对温度:合适的 SI 单位是开尔文。
常用形式
编辑最常引入的形式是: p V = n R T = n k B N A T = N k B T {displaystyle pV=nRT=nk_{TeXt{B}}N_{text{A}}T=Nk_{ text{B}}T} 其中:
- p {displaystyle p} 是气体的绝对压力,
- V {displaystyle V} 是气体的体积,
- n {displaystyle n} 是气体物质的量(也称为摩尔数),
- R {displaystyle R} 是理想的或通用的气体常数,等于玻尔兹曼常数和阿伏加德罗常数的乘积,
- k B {displaystyle k_{text{B}}} 是玻尔兹曼常数,
- N A {displaystyle N_{A}} 是阿伏加德罗常数,
- T {displaystyle T} 是气体的绝对温度,
- N {displaystyle N} 是气体粒子(通常是原子或分子)的数量。
在 SI 单位中,p 的单位是帕斯卡,V 的单位是立方米,n 的单位是摩尔,T 的单位是开尔文(开尔文温标是一种移动的摄氏温标,其中 0.00 K = −273.15 °C,可能的最低温度 ). R 的值为 8.314 J/(mol·K) = 1.989 ≈ 2 cal/(mol·K),或 0.0821 L·atm/(mol·K)。
摩尔形式
编辑可以通过给出质量而不是气体的化学量来指定存在多少气体。 因此,理想气体定律的另一种形式可能会有用。 化学量 n(以摩尔为单位)等于气体的总质量 (m)(以千克为单位)除以摩尔质量 M(以千克/摩尔为单位):
n = m M 。 {displaystyle n={frac {m}{M}}。}
通过用 m/M 替换 n 并随后引入密度 ρ = m/V,我们得到:
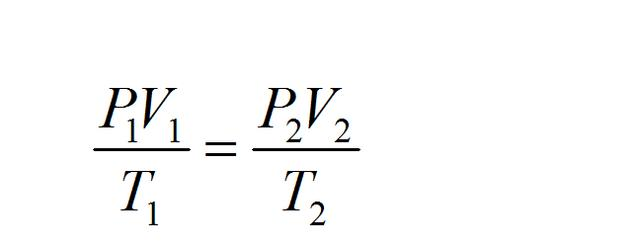
将特定气体常数 Rspecific(r) 定义为比率 R/M,
p = ρ R specific T {displaystyle p=rho R_{text{specific}}T}
这种形式的理想气体定律非常有用,因为它将压力、密度和温度联系在一个独特的公式中,与所考虑的气体的数量无关。
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/216123/
