- 1 弯曲的分子几何学
弯曲的分子几何学
编辑在化学中,两个相邻键的非直线排列的分子具有弯曲的分子几何学,也称为角形或V形。某些原子,如氧,由于其电子构型,几乎总是将其两个(或多个)共价键设置为非直角方向。水(H2O)是弯曲分子的一个例子,也是其类似物。两个氢原子之间的键角约为104.45°。其他三原子分子和只含有主族元素的离子也经常观察到非线性几何,突出的例子是二氧化氮(NO2)、二氯化硫(SCl2)和亚甲基(CH2)。这种几何形状几乎总是与VSEPR理论一致,该理论通常解释存在孤对的原子的非共轭性。弯曲有几种变体,其中最常见的是AX2E2,其中中心原子(A)的两个共价键和两个孤对形成一个完整的8电子壳。它们的中心角从104°到109.5°不等,其中后者与预测四个SP3杂化轨道的四面体对称性的简单化理论相一致。
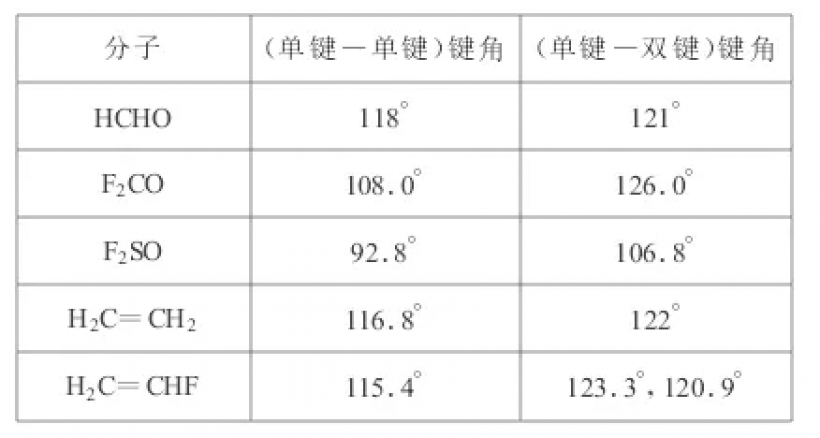
最常见的实际角度是105°、107°和109°:由于外围原子(X)的不同特性,它们会有所不同。其他情况也会出现轨道杂化,但程度不同。AX2E1分子,如SnCl2,只有一个孤对,中心角约为120°(等边三角形的中心和两个顶点)。它们有三个sp2轨道。也存在没有孤对的过渡金属的sd-杂化AX2化合物:它们的中心角约为90°,也被归类为弯曲的。(见VSEPR理论的进一步讨论#具有强d-贡献的化合物)。
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/160718/
