等熵过程
编辑在热力学中,等熵过程是理想化的热力学过程,它既是绝热的又是可逆的。 系统的功传递是无摩擦的,没有热量或物质的净传递。 这种理想化过程在工程中作为实际过程的模型和比较基础很有用。 这个过程是理想化的,因为现实中不会发生可逆过程; 将一个过程视为绝热和可逆过程将表明初始熵和最终熵是相同的,因此,它被称为等熵(熵不变)的原因。 热力学过程是根据它们对系统的影响来命名的。 尽管在现实中不一定可以进行等熵过程,但有些过程可以近似为等熵过程。
等熵这个词可以用另一种方式来解释,因为它的含义可以从它的词源中推导出来。 表示系统熵不变的过程; 如前所述,如果过程既是绝热又是可逆的,则可能会发生这种情况。 然而,这也可能发生在系统中所做的工作包括系统内部摩擦的系统中,并且从系统中提取适量的热量以补偿内部摩擦,从而使熵保持不变。 然而,相对于宇宙,宇宙的熵会因此增加,符合热力学第二定律。
背景
编辑热力学第二定律指出
T surr d S ≥ δ Q ,
其中 δ Q 是系统通过加热获得的能量,T surr 是周围环境的温度,d S 是熵的变化。 等号指的是一个可逆过程,这是一个想象的理想化的理论极限,在物理现实中从未真正发生过,系统和环境的温度基本相等。 对于等熵过程,如果也是可逆的,则没有能量以热的形式传递,因为该过程是绝热的; δQ = 0。相反,如果过程是不可逆的,则系统内部会产生熵; 因此,为了在系统内保持恒定的熵,必须同时将能量作为热量从系统中移除。
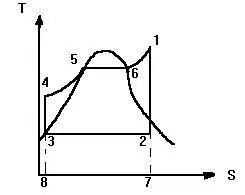
对于可逆过程,通过将系统与其周围环境隔热来进行等熵转变。 温度是熵的热力学共轭变量,因此共轭过程将是一个等温过程,其中系统与恒温热浴热连接。
热力学系统中的等候过程
编辑在内部可逆和绝热的过程中,给定质量的熵不会改变。 熵保持不变的过程称为等熵过程,写作 Δ s = 0 或 s 1 = s 2 . 理论上等熵热力学装置的一些例子是泵、气体压缩机、涡轮机、喷嘴和扩散器。
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/216643/
