简介
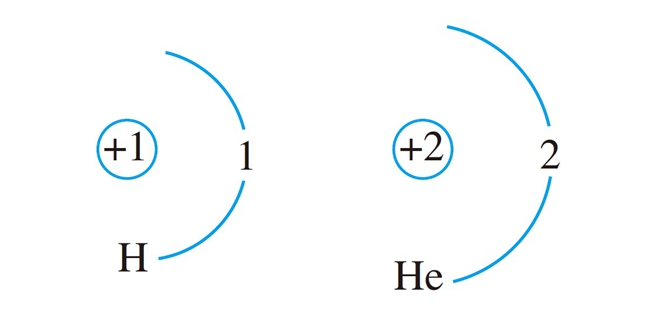
编辑二氢阳离子或氢分子离子为阳离子(正离子),分子式为H+2。 它由共享一个电子的两个氢原子核(质子)组成。 是最简单的分子离子。
离子可以由中性氢分子 H2 的电离形成。 它通常在宇宙射线的作用下在太空中的分子云中形成。
二氢阳离子具有重大的历史和理论意义,因为它只有一个电子,描述其结构的量子力学方程可以以相对简单的方式求解。 第一个这样的解决方案是由 Ø 推导出来的。 Burrau 在 1927 年,也就是量子力学波动理论发表仅一年后。
物理性质
编辑H+2 中的成键可以描述为共价单电子键,正式键级为二分之一。
离子的基态能量为 -0.597 Hartree。
同位素体
编辑二氢阳离子有六个同位素体,它们是由一个或多个质子被其他氢同位素的原子核取代而产生的; 即氘核(deuterons,2H+)或氚核(tritons,3H+)。
- H+2 = 1H+2(普通的)。
- D+2 = 2H+2(二氘阳离子)。
量子力学分析
编辑由于缺乏电子-电子排斥(电子相关),该阳离子的薛定谔方程(在钳位核近似中)可以以相对简单的方式求解。 电子能量特征值的解析解是 LamBERT W 函数的推广,可以在实验数学方法中使用计算机代数系统获得。 因此,它在大多数量子化学教科书中都作为示例包含在内。
H+2 的第一个成功的量子力学处理于 1927 年由丹麦物理学家 Øyvind Burrau 发表,距 Erwin Schrödinger 出版的波动力学。 Karel Niessen 和 Wolfgang Pauli 于 1922 年以及 Harold Urey 于 1925 年发表了使用旧量子理论的早期尝试。 1928 年,Linus Pauling 发表了一篇综述,将 Burrau 的工作与 Walter Heitler 和 Fritz London 在氢分子方面的工作放在一起。
钳位核(Born-Oppenheimer)近似
编辑氢分子离子 H+ 的电子薛定谔波动方程 2 有两个固定的核中心,标记为 A 和 B,一个 电子可以写成
( − ℏ 2 2 m ∇ 2 + V ) ψ = E ψ , {dISPlaystyle left(-{frac {hbar {2}}{2m}}nabla {2}+V 右)psi =Epsi ~,}
其中 V 是电子-核库仑势能函数:
V = − e 2 4 π ε 0 ( 1 r a + 1 r b ) {diSPlaystyle V=-{frac {e{2}}{4pi varepsilon _{0}}}left ({frac {1}{r_{a}}}+{frac {1}{r_{b}}}右)}
E 是给定量子力学状态(本征态)的(电子)能量,电子状态函数 ψ = ψ(r) 取决于电子的空间坐标。 附加项 1/R 对于固定的核间距离 R 是常数,已从势 V 中省略,因为它仅移动特征值。 电子和原子核之间的距离表示为 ra 和 rb。 在原子单位 (ħ = m = e = 4πε0 = 1) 波动方程是
( − 1 2 ∇ 2 + V ) ψ = E ψ 其中 V = − 1 r a − 1 r b 。 {displaystyle left(-{tfrac {1}{2}}nabla {2}+Vright)psi =Epsi QQuad {mbox{with} }qquad V=-{frac {1}{r_{a}}}-{frac {1}{r_{b}}};.}
我们选择原子核之间的中点作为坐标原点。 根据一般对称性原理,波函数可以通过它们关于点群反转操作 i (r ↦ −r) 的对称行为来表征。 存在关于 i 对称的波函数 ψg(r),以及在此对称操作下反对称的波函数 ψu(r):
ψ g / u ( − r ) = ± ψ g / u ( r ) 。 {displaystyle psi _{g/u}(-{mathbf {r} })={}pm psi _{g/u}({mathbf {r} }) ;.}
这里出现的后缀 g 和 u 来自德语 gerade 和 ungerade,表示点群反转操作 i 下的对称行为。 它们的使用是指定双原子分子电子态的标准做法,而对于原子态,则使用术语偶数和奇数。
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/216223/
