能级
编辑一个量子力学系统或粒子被束缚——也就是说,在空间上被限制——只能呈现某些离散的能量值,称为能级。 这与可以具有任意能量的经典粒子形成对比。 该术语通常用于原子、离子或分子中电子的能级,它们受原子核电场的约束,但也可以指原子核的能级或分子中的振动或旋转能级。 具有这种离散能级的系统的能谱被称为是量子化的。
在化学和原子物理学中,电子壳层或主能级可以被认为是一个或多个电子围绕原子核的轨道。 离原子核最近的壳层称为1壳层(也称K壳层),其次是2壳层(或L壳层),然后是3壳层(或M壳层),依此类推离原子核越来越远。 壳层对应于主要量子数(n = 1、2、3、4 …),或者用 X 射线符号中使用的字母按字母顺序标记(K、L、M、N …)。
每个壳层只能包含固定数量的电子:第一个壳层最多可容纳两个电子,第二个壳层最多可容纳八个 (2 + 6) 个电子,第三个壳层最多可容纳 18 个 (2 + 6 + 10 ) 等等。 通式是第 n 个壳层原则上最多可以容纳 2n2 个电子。 由于电子被原子核吸引,因此只有当更多的内壳已经被其他电子完全填充时,原子的电子通常才会占据外壳。 然而,这并不是一个严格的要求:原子可能有两个甚至三个不完整的外壳。 (有关更多详细信息,请参阅马德隆规则。)有关为什么电子存在于这些壳中的解释,请参阅电子配置。
如果势能在距离原子核或分子无限远的地方设置为零,通常的惯例是,束缚电子态具有负势能。
如果原子、离子或分子处于可能的最低能级,则称它及其电子处于基态。 如果它处于更高的能级,则称它被激发,或者任何能量高于基态的电子都被激发。 如果有不止一个可测量的量子力学状态与之相关,则一个能级被认为是退化的。
解释
编辑量子化的能级是由粒子的波动行为产生的,它给出了粒子能量与其波长之间的关系。 对于原子中的电子等受限粒子,具有明确能量的波函数具有驻波的形式。 具有明确能量的状态称为静止状态,因为它们是不随时间变化的状态。 非正式地,这些状态对应于波函数沿着一条闭合路径(一条在它开始的地方结束的路径)的整数波长,例如围绕原子的圆形轨道,其中波长的数量给出了原子轨道的类型(0 对于 s 轨道,1 对于 p 轨道等等)。 从数学上说明能级如何产生的基本例子是盒子里的粒子和量子谐振子。
能态的任何叠加(线性组合)也是量子态,但这种态会随时间变化,并且没有明确定义的能量。 对能量的测量导致波函数坍缩,从而产生仅由单一能态组成的新状态。 测量物体可能的能级称为光谱学。
历史
编辑原子量子化的第一个证据是约瑟夫·冯·弗劳恩霍夫和威廉·海德·沃拉斯顿在 1800 年代早期观察到太阳光的光谱线。 能级的概念是1913年丹麦物理学家尼尔斯·玻尔在玻尔原子理论中提出的。 1926 年,埃尔温·薛定谔和维尔纳·海森堡提出了用薛定谔方程解释这些能级的现代量子力学理论。
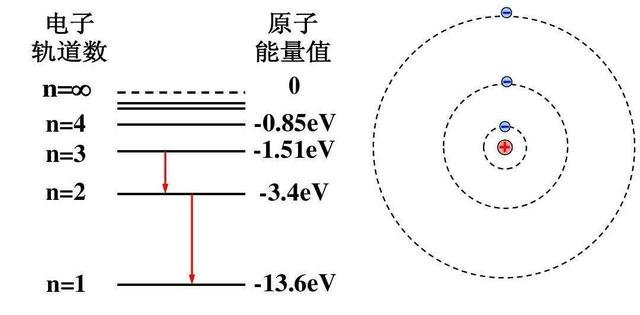
原子
编辑内在能量水平
编辑在下面给出的原子中各能级电子的能量公式中,当所讨论的电子完全离开原子时,即当电子的主量子数n = ∞时,能量为零点。 当电子以更接近的 n 值与原子结合时,电子的能量较低,被认为是负的。
轨道态能级:带核的原子/离子+一个电子
假设在类氢原子(离子)的给定原子轨道上有一个电子。 其状态的能量主要由(负)电子与(正)核的静电相互作用决定。 原子核周围电子的能级由下式给出:
E n = − h c R ∞ Z 2 n 2 {dISPlaystyle E_{n}=-hcR_{infty }{frac {Z{2}}{n{2}}}}
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/216231/
