渗透浓度
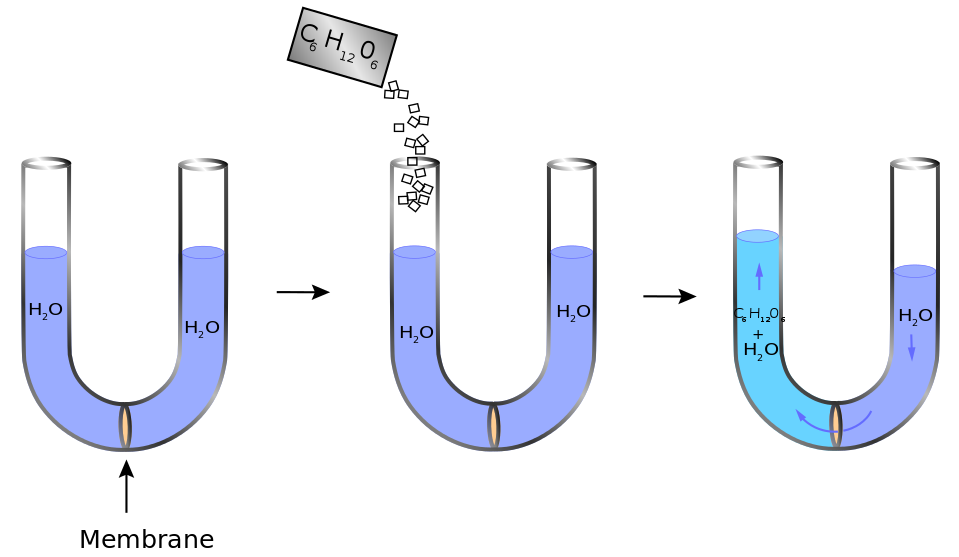
编辑渗透压浓度,以前称为渗透压,是溶质浓度的量度,定义为每升(L)溶液中溶质的渗透压(Osm)数(osmol/L或Osm/L)。溶液的渗透压通常表示为Osm/L(发音为osmolar),就像溶液的摩尔浓度表示为M(发音为摩尔)一样。摩尔浓度测量每单位体积溶液的溶质摩尔数,而渗透压测量每单位体积溶液中溶质颗粒的渗透摩尔数。该值允许测量渗透压解决方案和确定溶剂将如何扩散通过半透膜(渗透)分离两种不同渗透浓度的溶液。
单位
编辑渗透浓度的单位是渗透压。这是一个非SI测量单位,它定义了对溶液渗透压有贡献的溶质摩尔数。一毫渗透摩尔(mOsm)是渗透压的1/1,000。微渗透压(μOsm)(也拼写为微渗透压)是渗透压的1/1,000,000。
溶质类型
编辑渗透压不同于摩尔浓度,因为它测量的是溶质颗粒的渗透压,而不是溶质的摩尔数。之所以出现这种区别,是因为一些化合物可以在溶液中解离,而另一些则不能。
离子化合物,例如盐,可以在溶液中解离成它们的组成离子,因此溶液的摩尔浓度和同渗摩尔浓度之间没有一对一的关系。例如,氯化钠(NaCl)分解成Na+和Cl-离子。因此,对于溶液中每1摩尔NaCl,有2个osmoles的溶质颗粒(即1mol/LNaCl溶液是2osmol/LNaCl溶液)。钠离子和氯离子都会影响溶液的渗透压。
另一个例子是氯化镁(MgCl2),它分解成Mg2+和2Cl-离子。溶液中每1摩尔MgCl2就有3个渗透压的溶质颗粒。
非离子化合物不会离解,每1摩尔溶质仅形成1个渗透压溶质。例如,1mol/L的葡萄糖溶液为1osmol/L。
多种化合物可能有助于溶液的渗透压。例如,3Osm溶液可能包括:3摩尔葡萄糖,或1.5摩尔NaCl,或1摩尔葡萄糖+1摩尔NaCl,或2摩尔葡萄糖+0.5摩尔NaCl,或任何其他此类组合。
渗透压与张力
编辑渗透压和张力是相关但不同的概念。因此,以-osmotic结尾的术语(等渗、高渗、低渗)与以-tonic结尾的术语(等渗、高渗、低渗)不是同义词。这些术语是相关的,因为它们都比较了被膜隔开的两种溶液的溶质浓度。这些术语是不同的,因为渗透压考虑了渗透溶质和非渗透溶质的总浓度,而张力只考虑了非自由渗透溶质的总浓度。
渗透性溶质可以通过细胞膜扩散,当溶质拉动水分子时,会导致细胞体积发生瞬时变化。非穿透性溶质不能穿过细胞膜;因此,必须发生水穿过细胞膜的运动(即渗透)才能使溶液达到平衡。
溶液可以是高渗的和等渗的。例如,细胞内液和细胞外液可以是高渗的,但等渗的——如果一个隔室中溶质的总浓度与另一个不同,但其中一个离子可以穿过膜(换句话说,一种渗透性溶质),用它吸水,因此不会引起溶液体积的净变化。
血浆渗透压与渗透压
编辑血浆渗透压可以通过以下等式从血浆渗透压计算:
渗透压=渗透压*(ρsol−ca)
根据IUPAC,渗透压是水的有理活度的负自然对数与水的摩尔质量的商,而渗透压是渗透压和水的质量密度(也称为渗透浓度)的乘积。
简单来说,渗透压是每质量溶剂的溶质渗透浓度的表达,而渗透压是每体积溶液(因此通过乘以溶液中溶剂的质量密度(kg溶剂/升溶液)进行转换。
血浆渗透压/渗透压对于保持血流中适当的电解平衡很重要。不适当的平衡会导致脱水、碱中毒、酸中毒或其他危及生命的变化。抗利尿激素(加压素)通过控制身体在过滤血流时从肾脏保留的水量来部分负责这一过程。
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/135570/
