共价键
编辑共价键是一种化学键,涉及共享电子以在原子之间形成电子对。 这些电子对被称为共享对或键合对。 当原子共享电子时,原子之间吸引力和排斥力的稳定平衡称为共价键合。 对于许多分子,电子共享允许每个原子获得相当于一个完整的价壳层,对应于一个稳定的电子配置。 在有机化学中,共价键比离子键更常见。
共价还包括许多种相互作用,包括σ键、π键、金属与金属键、异质相互作用、弯曲键、三中心二电子键和三中心四电子键。 前缀 co- 表示联合、在行动中关联、在较小程度上合作等; 因此,共价键本质上意味着原子共享价,如价键理论中所讨论的那样。
在分子 H2 中,氢原子通过共价键共享两个电子。 电负性相似的原子之间的共价性最大。 因此,共价键不一定要求两个原子属于相同的元素,只需要它们具有相当的电负性即可。 需要在两个以上原子上共享电子的共价键被称为离域。
共价键的类型
编辑原子轨道(s 轨道除外)具有导致不同类型共价键的特定方向特性。 Sigma (σ) 键是最强的共价键,是由于两个不同原子上的轨道正面重叠所致。 单键通常是σ键。 Pi (π) 键较弱,是由于 p(或 d)轨道之间的横向重叠。 两个给定原子之间的双键由一个σ键和一个π键组成,三键由一个σ键和两个π键组成。
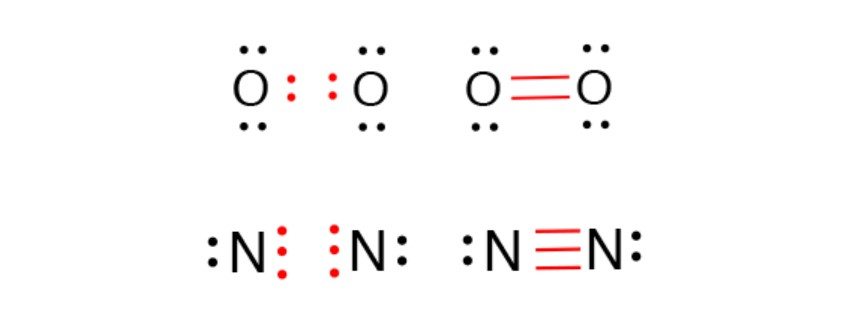
共价键还受到连接原子的电负性的影响,电负性决定了键的化学极性。 具有相同电负性的两个原子将形成非极性共价键,例如 H–H。 不相等的关系会产生极性共价键,例如 H−Cl。 然而,极性也需要几何不对称性,否则偶极子可能会相互抵消,从而产生非极性分子。
共价结构
编辑共价物质有几种结构类型,包括单个分子、分子结构、大分子结构和巨型共价结构。 单个分子具有将原子保持在一起的牢固键,但通常分子之间的吸引力可以忽略不计。
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/214677/
