碳-氧键
编辑碳-氧键是碳原子和氧原子之间的极性共价键。 碳-氧键存在于许多无机化合物中,如碳氧化物和卤氧化物、碳酸盐和金属羰基化合物,以及有机化合物,如醇、醚、羰基化合物和草酸盐。 氧有 6 个自己的价电子,并倾向于通过与其他原子共享电子形成共价键、接受电子形成阴离子或两者的组合,用 8 个电子填充其外壳。 在中性化合物中,一个氧原子最多可与碳形成两个单键或一个双键,而一个碳原子最多可与氧形成四个单键或两个双键。
结合基序
编辑氧键合
编辑在醚中,氧与两个碳原子形成两个共价单键,C-O-C,而在醇中,氧与碳形成一个单键,与氢形成一个单键,C-O-H。 在羰基化合物中,氧与碳形成共价双键,C=O,称为羰基。 在醚类、醇类和羰基化合物中,氧外壳中的四个非键合电子形成两个孤电子对。 在醇盐中,氧与碳形成单键并接受来自金属的电子以形成具有三个孤对的醇盐阴离子R-O-。 在氧鎓离子中,氧的两个孤对电子中的一个用于形成第三个共价键,生成阳离子 >O+– 或 =O+– 或 ≡O+,并保留一个孤电子对。
碳键
编辑碳原子在醇、醚和过氧化物中与氧形成一个单键,在缩醛中形成两个,在原酸酯中形成三个,在原碳酸酯中形成四个。 碳在醛、酮和酰卤中与氧形成双键。 在羧酸、酯和酸酐中,每个羰基碳原子与氧形成一个双键和一个单键。 在碳酸酯和碳酸中,羰基碳与氧形成一个双键和两个单键。 在二氧化碳中,碳与氧形成两个双键。
电负性和键长
编辑C–O 键强烈极化为氧(C 与 O 的电负性,2.55 与 3.44)。 石蜡基 C-O 键的键长在 143 pm 的范围内——小于 C-N 或 C-C 键。 由于部分双键特征,在羧酸中发现缩短的单键 (136 pm),在环氧化物中发现延长的键 (147 pm)。 C-O 键强度也大于 C-N 或 C-C。 例如,键合强度在甲醇中为 91 千卡 (380 kJ)/mol(在 298 K 时),在甲胺中为 87 千卡 (360 kJ)/mol,在乙烷中为 88 千卡 (370 kJ)/mol。
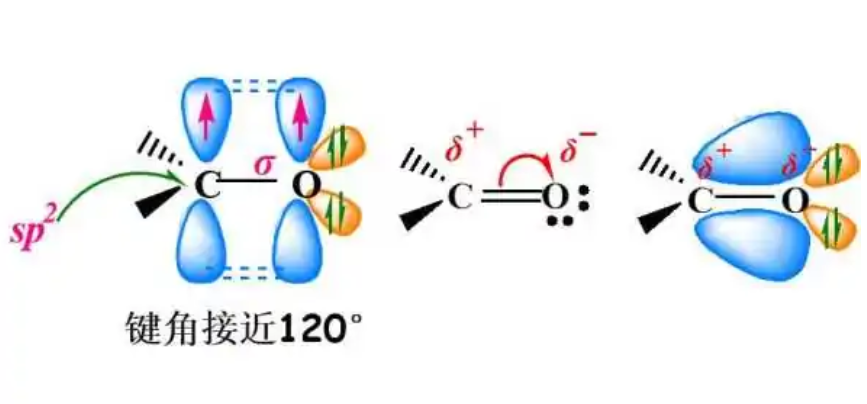
碳和氧在统称为羰基化合物的官能团中形成末端双键,这些化合物属于酮、酯、羧酸等化合物。 内部 C=O 键存在于带正电的氧鎓离子中。 在呋喃中,氧原子通过其填充的 p 轨道有助于 pi 电子离域,因此呋喃是芳香族的。 在羰基化合物中,C=O 键的键长约为 123 pm。 二氧化碳中的 C=O 键长为 116 pm。
酰卤中的 C=O 键具有部分三键特征,因此非常短:117 pm。 除了具有非常短的强键(112.8 pm)的一氧化碳和酰基离子 R–C≡O+(通常为 110-112 pm)之外,不存在具有正式 C≡O 三键的化合物。 这种三键具有非常高的键能,甚至高于 N-N 三键。 氧也可以是三价的,例如三乙基氧鎓四氟硼酸盐。
化学
编辑碳-氢键形成反应是威廉姆森醚合成、亲核酰基取代和烯烃的亲电加成反应。 Paternò–Büchi 反应涉及羰基化合物。
含氧官能团
编辑碳-氧键存在于这些功能组中
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/214665/
