多肽合成
编辑在有机化学中,肽合成是肽的生产,肽是多个氨基酸通过酰胺键(也称为肽键)连接的化合物。 肽是通过一个氨基酸的羧基与另一个氨基酸的氨基的缩合反应化学合成的。 保护基策略通常是必要的,以防止与各种氨基酸侧链发生不良副反应。 化学肽合成通常从肽的羧基末端(C 末端)开始,然后向氨基末端(N 末端)前进。 生物体中的蛋白质生物合成(长肽)发生在相反的方向。
肽的化学合成可以使用经典的液相技术进行,尽管这些技术在大多数研究和开发环境中已被固相方法所取代(见下文)。 然而,液相合成在工业用途的肽的大规模生产中仍然有用。
化学合成有助于生产难以在细菌中表达的肽、非天然氨基酸的掺入、肽/蛋白质主链修饰以及由 D-氨基酸组成的 D-蛋白质的合成。
固相合成
编辑在实验室中生产合成肽的既定方法称为固相肽合成 (SPPS)。 Spps 由 RoBERT Bruce Merrifield 首创,通过氨基酸衍生物在宏观不溶性溶剂溶胀珠状树脂支持物上的连续反应,可以快速组装肽链。
固体支持物由连接到新生肽链的反应基团(如胺基或羟基)功能化的小聚合物树脂珠组成。 由于肽在整个合成过程中始终与支持物共价结合,因此可以通过洗涤和过滤去除多余的试剂和副产物。 这种方法避免了在每个反应步骤后从溶液中分离相对耗时的产物肽,而这在使用传统的液相合成时是必需的。
每个要与肽链 N 末端偶联的氨基酸必须在其 N 末端和侧链上使用适当的保护基团进行保护,例如 Boc(酸不稳定)或 Fmoc(碱不稳定),具体取决于侧链和 使用的保护策略(见下文)。
一般的 SPPS 程序是交替 N 端脱保护和偶联反应的重复循环之一。 可以在每个步骤之间清洗树脂。 首先将氨基酸偶联到树脂上。 随后,胺被脱保护,然后与下一个要添加的氨基酸的活化羧基偶联。 重复这个循环,直到合成了所需的序列。 SPPS 循环还可以包括加帽步骤,以阻止未反应的氨基酸末端发生反应。 在合成结束时,将粗肽从固体支持物上切下,同时使用三氟乙酸等试剂去除所有保护基团。 粗肽可以从非极性溶剂如乙醚中沉淀出来,以去除有机可溶性副产物。 可以使用反相 HPLC 纯化粗肽。 纯化过程,尤其是较长肽的纯化过程可能具有挑战性,因为必须去除累积量的大量次要副产物,这些副产物具有与所需肽产物相似的特性。 出于这个原因,所谓的连续色谱工艺(如 MCSGP)越来越多地用于商业环境中,以在不牺牲纯度的情况下最大限度地提高产量。
SPPS 受到反应产量的限制,通常 70 个氨基酸范围内的肽和蛋白质正在推动合成可及性的极限。 合成难度也取决于序列; 通常,容易聚集的序列(如淀粉样蛋白)很难制备。 可以通过使用连接方法(例如天然化学连接)来获得更长的长度,其中两个较短的完全脱保护的合成肽可以在溶液中连接在一起。
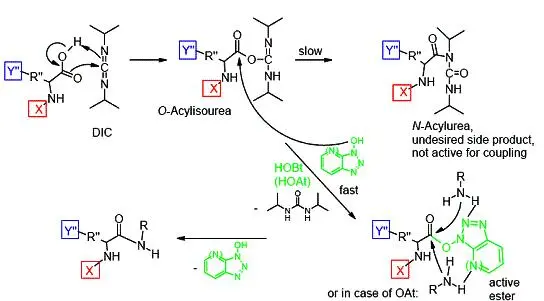
多肽偶联试剂
编辑使 SPPS 得到广泛应用的一个重要特征是在偶联步骤中产生极高的产量。 需要高效的酰胺键形成条件。 并添加过量的每种氨基酸(2 到 10 倍)。 偶联过程中氨基酸外消旋化的最小化对于避免最终肽产品中的差向异构化也是至关重要的。
胺和羧酸之间的酰胺键形成很慢,因此通常需要“偶联剂”或“活化剂”。 存在范围广泛的偶联试剂,部分由于它们对特定偶联的不同有效性,许多这些试剂是可商购的。
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/228814/
