磷酸和磷酸盐
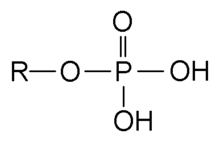
编辑一般意义上的磷酸是一种磷的氧化剂,其中每个磷(P)原子处于氧化态+5,并与四个氧(O)原子结合,其中一个通过双键,排列成四面体的角。两个或多个这样的PO4四面体可以通过共享的单键氧原子连接,形成线性或支链、循环,或更复杂的结构。没有共享的单键氧原子是用酸性氢原子完成的。磷酸的一般公式是Hn+2-2xPnO3n+1-x,其中n是磷原子的数量,x是分子结构中基本循环的数量,在0和(n+2)/2之间。从k个羟基中除去质子(H+)-OH,留下的阴离子一般称为磷酸盐(如果k=n-2x+2)或氢磷酸盐(如果k在1和n-2x+1之间),一般公式为[Hn-2x+2-kPnO3n+1-x]k-。完全解离的阴离子(k=n-2x+2)的公式为[PnO3n-x+1](n-2x+2)-是该术语也用于有机化学中,当或更多的氢被其他基团的键所取代时产生的官能团。这些酸,连同它们的盐和酯,包括一些最著名的磷化合物,在生物化学、矿物学、农业、药学、化学工业和化学研究中具有高度重要性。
酸类
编辑正磷酸盐最简单和最常遇到的磷酸是正磷酸盐,H3PO4。事实上,磷酸这个词经常特指这种化合物(这也是目前国际理论化学联合会的命名法)。寡磷酸盐和多磷酸盐两个或更多的正磷酸盐分子可以通过消除水而凝结成较大的分子。几个单位的缩合得到的是低聚磷酸,而较大的分子被称为多聚磷酸。(然而,这两个术语之间的区别并没有很好的定义)。例如,焦磷酸、三磷酸和四磷酸可以通过以下反应得到2H3PO4→H4P2O7+H2OH4P2O7+H3PO4→H5P3O10+H2OH5P3O10+H3PO4→H6P4O13+H2O多磷酸分子的主干是一条由P和O原子交替组成的链。每多凝结一个正磷单位,就多增加一个H(氢)原子、一个P(磷)原子和三个O(氧)原子。多磷酸盐的一般公式为Hn+2PnO3n+1或HO(-P(O)(OH)-O-)nH。多磷酸盐在有机合成中用于环化和酰化;另一个选择是伊顿试剂。环状磷酸同一分子的两个-OH单元之间的缩合,则是消除两个氢原子和一个氧原子,形成一个循环,如三甲基磷酸的形成。H5P3O10→H3P3O9+H2O磷酸的通式是Hn-2x+2PnO3n-x+1,其中n是磷原子的数目,x是分子结构中基本循环的数目;也就是说,为消除所有循环而必须断开的最小键数。正磷酸盐H3PO4焦磷酸H4P2O7三聚磷酸H5P3O10四聚磷酸H6P4O13三聚磷酸H3P3O9磷酸酐P4O10内部缩合的极限情况,即所有的氧原子都是共用的,没有氢原子(x=(n+2)/2),这将是一个酐PnO5n/2,如五氧化二磷P4O10。
磷酸盐
编辑去除作为质子的氢原子H+,使磷酸变成磷酸盐阴离子。部分去除会产生各种磷酸氢根阴离子。正磷酸盐正磷酸盐H3PO4的阴离子是正磷酸盐(通常称为简单的磷酸盐)PO3-4、一氢磷酸盐HPO2-4和二氢磷酸盐H2PO-4。线性低磷酸盐和多磷酸盐焦磷酸H4P2O7解离产生四个阴离子,H4-kP2O-7k-,其中电荷k从1到4不等。最后一个是焦磷酸盐[P2O4-7。焦磷酸盐大多是水溶性的。
同样,三聚磷酸H5P3O10产生至少五个阴离子[H5-kP3O10]k-,其中k的范围为1至5,包括三聚磷酸[P3O5-10。四聚磷酸H6P4O13产生至少六个阴离子,包括四聚磷酸[P4O6-13,以此类推。请注意,每一个额外的磷酸单元会增加一个额外的P原子、三个额外的O原子,以及一个额外的氢原子或一个额外的负电荷。分支的多磷酸会产生类似的分支的多磷酸盐阴离子。最简单的例子是磷酸三磷酸盐[OP(OPO3)3]9-及其部分解离的版本。此类(非环状)多磷酸盐阴离子的一般公式为[Hn+2-kPnO3n+1]k-,其中电荷k可从1到n+2不等。一般来说,在水溶液中,解离的程度或百分比取决于溶液的pH值。环状多磷酸盐磷酸单元可以以下列方式结合在一起
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/156746/
