氢化钠
编辑氢化钠是经验式为NaH的化学化合物。这种碱金属氢化物主要在有机合成中作为一种强而可燃的碱。NaH是一种盐类(类似盐)氢化物,由Na+和H-离子组成,与硼烷、甲烷、氨和水等分子氢化物不同。它是一种不溶于有机溶剂的离子性物质(尽管可溶于熔融的Na),这与H-离子不存在于溶液中的事实相一致。由于NaH的不可溶性,所有涉及NaH的反应都发生在固体的表面。
基本特性和结构
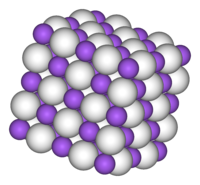
编辑氢气是由氢气和液态钠直接反应产生的。纯净的NaH是无色的,但样品一般呈现灰色。氢氧化钠的密度比Na(0.968克/立方厘米)高约40%。NaH,像LiH、KH、RbH和CsH一样,采用NaCl晶体结构。在这个图案中,每个Na+离子被六个H-中心以八面体的几何形状包围。根据Na-H和Na-F的距离判断,H-(NaH中为146pm)和F-(133pm)的离子半径是相当的。
反氢化钠
编辑一种非常不寻常的情况发生在一种被称为反氢化钠的化合物中,它含有H+和Na-离子。Na-是一种碱化物,这种化合物与普通的氢化钠不同,由于两个电子从氢到钠的净位移,其能量含量高得多。这种反式氢化钠的衍生物在碱[36]adamanzane的存在下产生。这个分子不可逆地封装了H+,并屏蔽了它与碱式钠的相互作用。理论工作表明,即使是未受保护的质子化叔胺与碱化钠络合,在某些溶剂条件下也可能是可转移的,尽管反应的障碍很小,找到合适的溶剂可能很困难。
在有机合成中的应用
编辑作为一种强碱,NaH在有机化学中具有广泛的范围和用途。作为一种超级碱,它能够使一系列甚至是弱的布朗斯特酸去质子化,从而得到相应的钠衍生物。典型的简单底物含有O-H、N-H、S-H键,包括醇类、酚类、吡唑类和硫醇。NaH明显去质子化碳酸(即C-H键),如1,3-二羰基,如丙二酸酯。由此产生的钠衍生物可以被烷基化。NaH广泛用于促进通过Dieckmann缩合、Stobbe缩合、Darzens缩合和Claisen缩合的羰基化合物的缩合反应。其他容易被NaH去质子化的碳酸包括硫铵盐和DMSO。氢氧化钠可用于制造硫磺酰亚胺,而硫磺酰亚胺又可用于将酮类转化为环氧化物,如约翰逊-科里-柴可夫斯基反应。作为还原剂,NaH可以还原某些主族化合物,但类似的反应性在有机化学中非常罕见(见下文)。值得注意的是,三氟化硼反应产生二硼烷和氟化钠。6NaH+2BF3→B2H6+6NaF二烷和二硫化物中的Si-Si和S-S键也被还原。由氢化钠和碱金属碘化物(NaH⋅MI,M=Li,Na)组成的复合试剂可以实现一系列的还原反应,包括三级腈类的加氢脱氰,亚胺还原为胺,以及酰胺还原为醛。
储氢
编辑尽管氢化钠在商业上并不重要,但已被建议用于燃料电池汽车的储氢。在一个实验中,含有氢化钠的塑料颗粒在有水的情况下被压碎以释放氢气。这项技术的一个挑战是如何从NaOH中再生NaH。
氢化钠现状
编辑氢化钠是以60%的氢化钠(w/w)在矿物油中的混合物形式出售。这样的分散体在处理和称重上都比纯氢化钠更安全。这种化合物经常以这种形式使用,但纯灰色固体可以通过用戊烷或四氢呋喃冲洗商业产品来制备,但要注意,因为废溶剂中含有微量的氢化钠,在空气中会被点燃。涉及NaH的反应需要无空气技术。通常情况下,NaH在四氢呋喃中作为悬浮液使用,这种溶剂可以抵抗强碱的侵蚀,但可以溶解许多反应性钠化合物。安全的NaH在空气中可以自发点燃。它还会与水剧烈反应,释放出氢气(也是易燃物)和氢氧化钠(NaOH)(一种苛性碱)。在实践中,大多数氢化钠是以油的分散体形式分配的,可以在空气中安全处理。
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/156814/
