四氧化三铁(英文名:Triiron tetraoxide),别名铁黑、磁性氧化铁,化学式Fe₃O₄,是氧化铁(Fe₂O₃)和氧化亚铁(FeO)的加成物,Fe₃O₄中的铁离子1/3是Fe²⁺,2/3是Fe³⁺。四氧化三铁常态为黑色立方系结晶或无定形粉末,其熔点为1594 ℃,此温度下会分解,密度5.17 g/cm³,不溶于水和有机溶剂,有强磁性,遮盖力和着色力强。天然磁铁矿中的四氧化三铁性质稳定,有良好的耐碱性,溶于浓酸、热强酸。Fe₃O₄的制备方法有共沉淀法、水热溶剂法、微乳液法等,在环境、生物医学、能源和材料等多个领域均有应用。
发现历史
编辑天然磁石的主要成分是四氧化三铁,公元前6-7世纪,中西方都各自发现了天然磁石吸铁现象,中国人由此发明了司南、指南针并应用于航海,影响了人类文明的发展。人类最早对四氧化三铁的理解开始于19世纪早期,化学分析表明这种磁性材料的分子组成为Fe₃O₄。最早布拉格(Bragg)称四氧化三铁具有立方尖晶石结构,后来韦尔维(Verwey)和布尔(Boer)经过分析,认为四氧化三铁有反尖晶石结构。1948年,尼尔(Neel)推进了亚铁磁性理论。1984年,Yanase和Siratori通过能带结构计算研究,发现具有立方尖晶石结构的四氧化三铁是稀少的具有多数自旋方向带隙的半金属铁磁体。2002年,Mortonx通过自旋极化光发射谱法测量了四氧化三铁的自旋极化率为-40%,四氧化三铁的电运输特性被人们广泛研究。
分布情况
编辑自然界中四氧化三铁主要存在于磁铁矿中,磁铁矿在世界范围内都有分布,中国、俄罗斯、美国、澳大利亚、巴西等国家均有丰富的磁铁矿矿藏,瑞典的基鲁纳、智利的拉克铁矿都是有名的磁铁矿产地。
物质结构
编辑四氧化三铁是Fe²⁺、Fe³⁺、O²⁻组成的反尖晶石结构离子晶体,晶体由O²⁻组成含四面体空隙和八面体空隙的骨架,Fe²⁺、Fe³⁺填充在O²⁻形成的多面体空隙中。具体结构如图下所示:
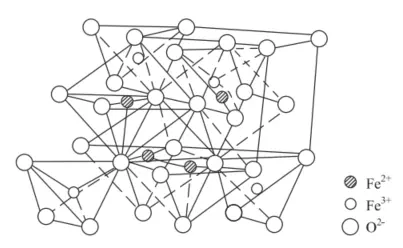
理化性质
编辑物理性质
四氧化三铁外观为黑色立方系结晶或无定形粉末,其熔点为1594 ℃,此温度下会分解,密度5.17 g/cm³,不溶于水和有机溶剂,有强磁性,遮盖力和着色力强。
化学性质
四氧化三铁不与碱反应,溶于浓酸、热强酸,能够被强还原剂还原或被强氧化剂氧化。
与酸反应
氧化还原反应
四氧化三铁能被氢气、铝、碳等单质和一氧化碳还原成铁或氧化亚铁。
四氧化三铁能被氧气氧化成三氧化二铁,被重铬酸钾的酸性溶液氧化成三价铁盐。
制备方法
编辑四氧化三铁的生产方法从工艺上可分为湿法和干法。
湿法
直接合成法
直接合成法也叫加成法,做法是将三氧化二铁与氢氧化亚铁在一定的pH和温度下直接进行加成反应,而后经脱水、干燥、粉碎得到四氧化三铁。主要发生的化学反应如下:
氢氧化亚铁氧化法
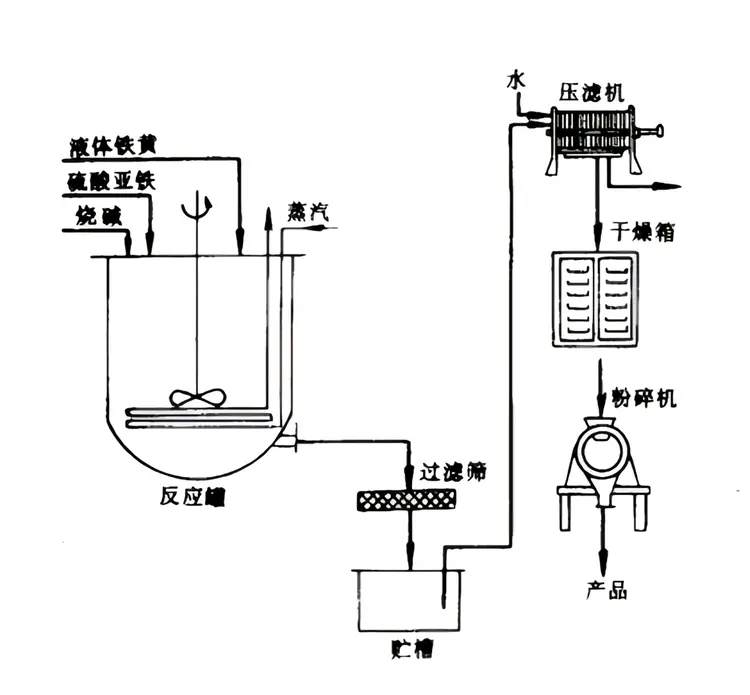
氢氧化亚铁氧化法的做法是在一定的pH和温度下,将氢氧化钠溶液和硫酸亚铁溶液混合反应生成氢氧化亚铁溶液。
氢氧化亚铁不稳定,随着反应的进行,在搅拌的作用下氧化亚铁会被空气氧化成绿锈,反应接近终点时,投入适量氧化剂硝酸铵并鼓入空气。
生成的铁黑沉淀经分离、干燥、粉碎即可获得四氧化三铁产品。
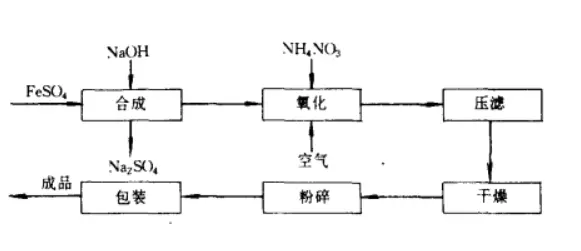
干法
干法制备四氧化三铁的做法是将粉碎后的三氧化二铁在严格控制的反应条件下还原成四氧化三铁。
纳米材料制备
四氧化三铁纳米粒子化学性质稳定,具有良好的磁响应性、耐候性、生物相容性等。可以通过共沉淀法、溶胶–凝胶法、热分解法、溶剂热法等方式生产。共沉淀法:一般做法是在Ar或N₂的保护下,使用铁盐[
,
等]和亚铁盐(
和
等)按比例配置成盐溶液,加入碱性沉淀剂(如
,
等),在一定的pH、温度等条件下进行共沉淀,可获得性能优良的
微粒。主要的反应原理为:
溶胶-凝胶法:做法是按比例将
溶液混合,调节溶液的pH后进行蒸发得到凝胶。热分解法的做法是将油铁酸、Fe(CO)₅、Fe(acac)等铁的有机配合物溶于高沸点有机溶剂,通过控制温度、反应时长、加反应活性剂等制备四氧化三铁。溶剂热法:采用醇、胺、酮[tóng]等作为溶剂,溶剂能够溶解反应物为反应提供液相环境同时也充当还原剂将三价铁还原成二价铁;加入的矿化剂使的反应能够进行,并且通过调整矿化剂能够改变四氧化三铁粒子的大小;调整表面活性剂的种类和浓度能够影响四氧化三铁粒子的形状。
应用领域
编辑环境领域
四氧化三铁的磁性纳米粒子比表面积极高,因此具有很好的吸附性能,在水处理,例如去除水中的重金属离子等方面有巨大优势;有磁性,在磁场的作用下能够从溶剂中快速分离并避免二次污染;有易修饰功能团,能对目标物产生特异性亲和吸附的效果。不过四氧化三铁磁性纳米颗粒也有其局限性,如裸露在空气中的四氧化三铁纳米颗粒极易氧化,容易因磁性发生团聚导致吸附性能下降等,所以需要对四氧化三铁纳米颗粒进行改性和修饰,以提升器对重金属离子的吸附效果。
生物医学领域
四氧化三铁有优异的生物相容性、低毒性,在医学领域可用于磁性靶向给药、生物标定、细胞标记、核磁造影等。比如在肿瘤治疗中,四氧化三铁纳米粒子能够增强肿瘤的核磁共振成像信号、用于热磁治疗、负载药物将药物输送至指定位置等。
材料领域
四氧化三铁具有特殊的光电磁效应,能够用于制作新型电子材料和特殊功能性材料,如制备磁性流体,磁性液体是含有众多纳米级的铁磁性或亚铁磁性微粒并且性质稳定的胶体溶液,是既有液体的流动力,又有固体的磁性的一种新型功能材料。这种磁性液体即便受到外界磁场、重力场等的作用也能长期稳定存在,被广泛应用于印刷、真空密封包装、传感器等领域中。四氧化三铁遮盖力高、着色力强、具有良好的耐碱性,可用于制作涂料、油墨、油彩等。
催化领域
四氧化三铁粒子具有巨大的比表面积,能够作为催化剂,例如催化有机合成反应、催化降解有机染料等,且因为其自身具有磁性,相较其他催化剂具有能够快速分离回收的优点;四氧化三铁纳米粒子还能充当催化剂的载体,方便催化剂的回收利用等,比如负载贵金属催化剂、有机化合物催化剂。
能源领域
四氧化三铁具有高理论电容、导电率高、价格低等优点,与其他材料复合后能够作为锂离子电池、超级电容器的电极材料,提高电池的性能。四氧化三铁还能够作为储氢材料,其反应机理为:储氢:
放氢:
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/1235435/
