疏水效应
编辑疏水效应是观察到的非极性物质在水溶液中聚集并排斥水分子的趋势。 疏水一词的字面意思是不怕水的,它描述了水和非极性物质的隔离,使水分子之间的氢键最大化,水和非极性分子之间的接触面积最小。 在热力学方面,疏水效应是水围绕溶质的自由能变化。 周围溶剂的正自由能变化表示疏水性,而负自由能变化表示亲水性。
疏水作用负责将油和水的混合物分离成两个组分。 它还负责与生物学相关的效应,包括:细胞膜和囊泡形成、蛋白质折叠、膜蛋白插入非极性脂质环境和蛋白质-小分子结合。 因此,疏水作用对生命至关重要。 观察到这种效应的物质称为疏水物。
两亲物
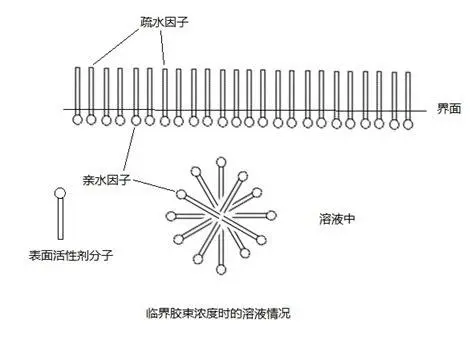
编辑两亲分子是同时具有疏水域和亲水域的分子。 洗涤剂由两亲物组成,这些两亲物允许疏水分子通过形成胶束和双层(如肥皂泡)溶解在水中。 它们对由两亲性磷脂组成的细胞膜也很重要,可防止细胞的内部水环境与外部水混合。
大分子的折叠
编辑在蛋白质折叠的情况下,疏水效应对于理解具有在蛋白质内聚集在一起的疏水氨基酸(例如甘氨酸、丙氨酸、缬氨酸、亮氨酸、异亮氨酸、苯丙氨酸、色氨酸和甲硫氨酸)的蛋白质的结构很重要。 水溶性蛋白质的结构具有疏水核心,其中侧链被水掩埋,从而稳定了折叠状态。 带电和极性侧链位于暴露于溶剂的表面上,它们与周围的水分子相互作用。 尽量减少暴露于水的疏水侧链的数量是折叠过程背后的主要驱动力,尽管蛋白质内氢键的形成也能稳定蛋白质结构。
DNA 三级结构组装的能量学被确定为由疏水效应驱动,此外还有 Watson-Crick 碱基配对(负责序列选择性)和芳香碱基之间的堆叠相互作用。
蛋白质纯化
编辑在生物化学中,疏水效应可用于根据疏水性分离蛋白质混合物。 具有疏水性固定相(例如苯基琼脂糖凝胶)的柱层析会导致疏水性更强的蛋白质移动更慢,而疏水性更差的蛋白质会更快地从色谱柱中洗脱出来。 为了实现更好的分离,可以添加盐(较高浓度的盐会增加疏水效果)并且随着分离的进行其浓度会降低。
原因
编辑疏水效应的起源尚不完全清楚。一些人认为疏水相互作用主要是一种熵效应,源于非极性溶质破坏液态水分子之间的高动态氢键。 大分子的烃链或类似的非极性区域不能与水形成氢键。 将这种非氢键表面引入水中会破坏水分子之间的氢键网络。 氢键重新定向为与该表面相切,以最大程度地减少水分子氢键 3D 网络的破坏,这导致在非极性表面周围形成结构化水笼。 形成笼(或包合物)的水分子流动性受限。
在小的非极性粒子的溶剂化壳中,限制达到大约 10%。 例如,在室温下溶解的氙的情况下,已发现 30% 的迁移率限制。 对于较大的非极性分子,溶剂化层中水分子的重新定向和平移运动可能会受到二到四倍的限制; 因此,在 25°C 时,水的重新定向相关时间从 2 皮秒增加到 4-8 皮秒。 通常,这会导致水分子平移和旋转熵的显着损失,并使该过程在系统中的自由能方面不利。 通过聚集在一起,非极性分子减少了暴露于水的表面积并最大限度地减少了它们的破坏作用。
疏水效应可以通过测量非极性分子在水和非极性溶剂之间的分配系数来量化。 分配系数可以转换为传输自由能,其中包括焓和熵分量,ΔG = ΔH – TΔS。
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/214695/
