简介
编辑转氨作用是一种化学反应,将一个氨基转移到一个酮酸上以形成新的氨基酸。这一途径负责大多数氨基酸的脱氨作用。这是主要的降解途径之一,将必需氨基酸转化为非必需氨基酸(可由生物体从头合成的氨基酸)。
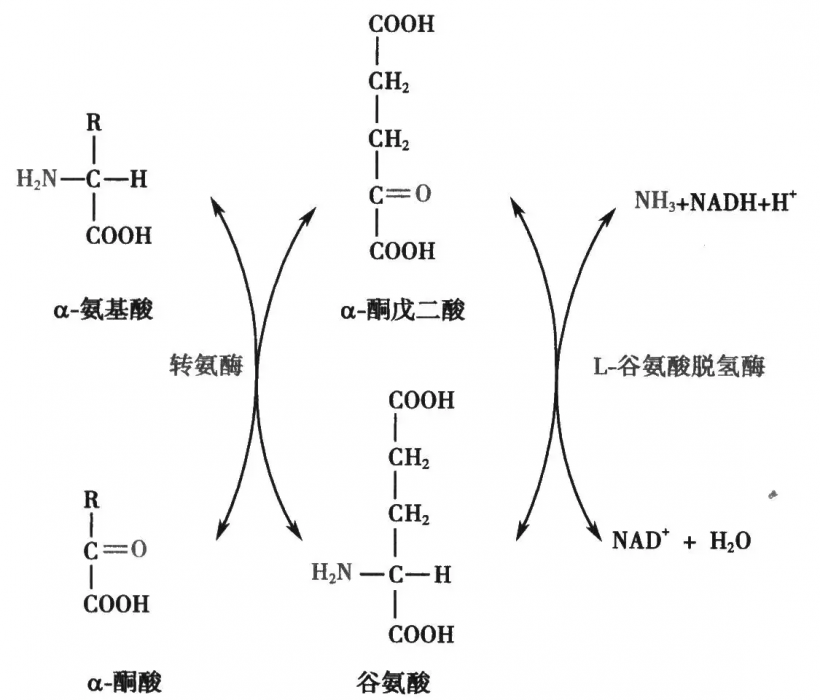
生物化学中的转氨作用是由称为转氨酶或转氨酶的酶完成的。α-酮戊二酸作为主要的氨基组受体,产生谷氨酸作为新的氨基酸。氨基酸+α-酮戊二酸↔α-酮酸+谷氨酸谷氨酸的氨基又在第二次转氨反应中转移到草酰乙酸,产生天门冬氨酸。谷氨酸+草酰乙酸↔α-酮戊二酸+天冬氨酸
作用机制
编辑由转氨酶催化的转氨反应发生在两个阶段。在第 一步,一个氨基酸的α氨基被转移到酶上,产生相应的α-酮酸和胺化的酶。在第二阶段,氨基被转移到酮酸接受体上,形成氨基酸产品,同时使酶再生。
氨基酸的手性是在转氨过程中确定的。为了完成反应,氨基转移酶需要含醛辅酶的参与,5′-磷酸吡哆醇(PLP),吡哆醇(维生素B6)的衍生物。氨基是通过将这种辅酶转化为吡哆醇-5′-磷酸(PMP)而被容纳的。PLP通过其醛基与酶Lys残基的ε-氨基缩合而形成的席夫碱连接共价连接到酶上。与酶的吡啶环共轭的希夫碱是辅酶活性的重点。
转氨反应的产物取决于α-酮酸的可用性。产品通常是丙氨酸、天门冬氨酸或谷氨酸,因为它们相应的α-酮酸是通过燃料的代谢产生的。作为一个主要的降解氨基酸途径,赖氨酸、脯氨酸和苏氨酸是仅有的三种不总是进行转氨的氨基酸,而是使用各自的脱氢酶。
替代机制第二类转氨反应可以描述为一个胺或酰胺阴离子对一个胺或铵盐的亲核取代。例如,一个一级胺被一个一级酰胺阴离子攻击可以用来制备二级胺:RNH2+R’NH-→RR’NH+NH2-可以用雷尼镍制备对称的二级胺(2RNH2→R2NH+NH3)。最后,季铵盐可以用乙醇胺进行脱烷基:R4N++NH2CH2CH2OH→R3N+RN+H2CH2CH2OH氨基萘也会发生转氨反应[2]。
转氨酶的类型
编辑转氨是由几种不同的转氨酶介导的。这些酶可能对单个氨基酸具有特异性,也可能能够处理一组化学上相似的氨基酸。后者适用于支链氨基酸组,其中包括亮氨酸、异亮氨酸和缬氨酸。两种常见的转氨酶是丙氨酸转氨酶(ALT)和天冬氨酸转氨酶(AST)。
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/160659/
