药物设计
编辑药物设计(通常称为合理药物设计或简称合理设计)是基于生物学靶点知识寻找新药物的创造性过程。该药物最常见的是激活或抑制生物分子(如蛋白质)功能的有机小分子,从而对患者产生治疗益处。从最基本的意义上讲,药物设计涉及形状和电荷互补的分子设计 与它们相互作用的生物分子靶标结合,因此将与之结合。药物设计经常但不一定依赖于计算机建模技术。这种类型的建模有时称为计算机辅助药物设计。最后,依赖于生物分子靶标的三维结构知识的药物设计被称为基于结构的药物设计。除小分子外,生物药物还包括肽,尤其是治疗性抗体药物是越来越重要的一类,并且已经开发出用于改善这些基于蛋白质的治疗剂的亲和力,选择性和稳定性的计算方法。
短语“药物设计”在某种程度上是错误的称呼。一个更准确的术语是配体设计(即与目标紧密结合的分子设计)。尽管预测结合亲和力的设计技术相当成功,但还有许多其他特性,例如生物利用度、代谢半衰期、副作用等,必须首先进行优化,然后配体才能变得安全有效。药品。这些其他特征通常很难通过合理的设计技术来预测。然而,由于高流失率,特别是在临床阶段的药物开发,在药物设计过程的早期,人们将更多的注意力集中在选择候选药物上,这些候选药物的理化特性预计在开发过程中将减少并发症,因此更有可能导致批准上市的药物。此外,在早期药物发现中,越来越多地使用具有计算方法的体外实验来选择具有更有利的ADME(吸收、分布、代谢和排泄)和毒理学特征的化合物。
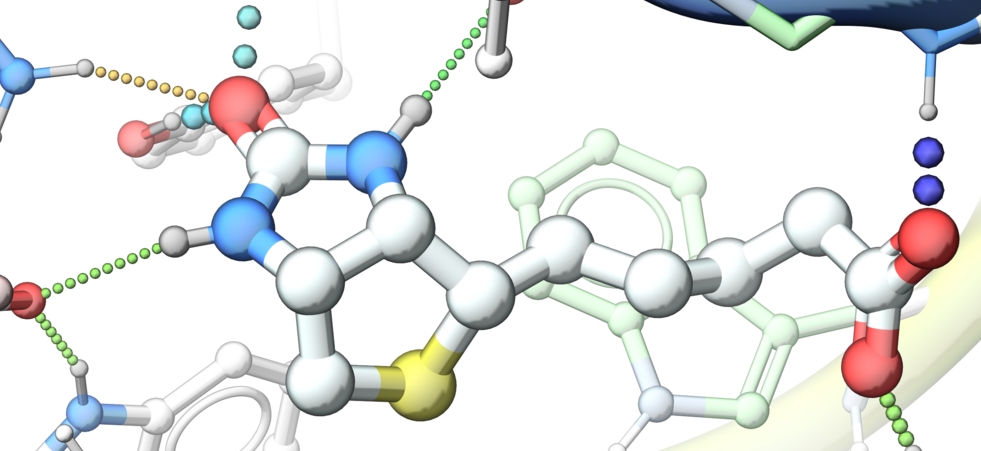
计算机辅助药物设计
编辑药物设计的最基本目标是预测给定分子是否会与靶标结合,以及结合强度如何。 分子力学或分子动力学最常用于估算小分子与其生物学靶标之间分子间相互作用的强度。这些方法还用于预测小分子的构象,并模拟当小分子与其结合时可能发生的靶标构象变化。半经验,从头算量子化学方法或密度泛函理论 通常用于为分子力学计算提供优化的参数,并提供可能影响结合亲和力的候选药物的电子性质(静电势、极化率等)的估计值。
分子力学方法也可用于提供结合亲和力的半定量预测。同样,基于知识的评分功能可用于提供绑定亲和力估计。这些方法使用线性回归、机器学习、神经网络或其他统计技术,通过使实验亲和力适合计算得出的小分子与目标之间的相互作用能来推导预测的结合亲和力方程。
理想地,该计算方法将能够在合成化合物之前预测亲和力,因此理论上仅需要合成一种化合物,从而节省了大量时间和成本。现实情况是,当前的计算方法是不完善的,充其量只能提供定性上准确的亲和力估计。实际上,在发现最佳药物之前,仍然需要进行多次设计,合成和测试迭代。计算方法通过减少所需的迭代次数加快了发现速度,并经常提供新颖的结构。
借助计算机进行的药物设计可用于以下任何药物发现阶段:
- 使用虚拟筛选进行命中识别(基于结构或配体的设计)
- 击到引线亲和力和选择性的优化(基于结构的设计、QSAR等)
- 在保持亲和力的同时优化其他药物特性
为了克服最近的评分功能所计算的结合亲和力预测不足,将蛋白质-配体相互作用和化合物3D结构信息用于分析。对于基于结构的药物设计,已经开发了一些针对蛋白质-配体相互作用的后筛选分析,以改善富集并有效地挖掘潜在候选物:
- 共识评分
- 通过多种评分功能投票选择候选人
- 可能失去蛋白质-配体结构信息与评分标准之间的关系
- 聚类分析
- 根据蛋白质-配体3D信息表示和聚集候选对象
- 需要蛋白质-配体相互作用的有意义的表示。
药物设计的类型
编辑药物设计有两种主要类型。第一种称为基于配体的药物设计,第二种称为基于结构的药物设计。
基于配体的
编辑基于配体的药物设计(或间接药物设计)依赖于与目标生物学靶标结合的其他分子的知识。这些其他分子可用于推导药效团模型,该模型定义了分子必须具有的最低必需结构特征才能与靶标结合。换句话说,可以基于结合靶标的知识来建立生物靶标的模型,并且该模型又可以用于设计与靶标相互作用的新的分子实体。或者,定量结构-活性关系(QSAR),其中分子的计算特性与其实验确定的生物活性之间的相关性,可以得出。这些QSAR关系又可以用来预测新类似物的活性。
基于结构
编辑基于结构的药物设计(或直接药物设计)依赖于通过诸如X射线晶体学或NMR光谱学等方法获得的生物靶标的三维结构的知识。如果靶标的实验结构不可用,则有可能根据相关蛋白质的实验结构创建靶标的同源性模型。利用生物靶标的结构,可以使用交互式图形和医学化学家的直觉设计预测与靶标具有高亲和力和选择性结合的候选药物。可替代地,可以使用各种自动计算程序来建议新药物候选者。
当前基于结构的药物设计方法可大致分为三大类。第一种方法是通过搜索小分子3D结构的大型数据库来寻找给定受体的新配体,以使用快速近似对接程序找到适合受体结合口袋的那些。这种方法称为虚拟筛选。第二类是新配体的从头设计。在这种方法中,通过逐步组装小片段,在结合口袋的约束内建立了配体分子。这些片段可以是单个原子或分子片段。这种方法的主要优点是可以提出任何数据库中都没有的新颖结构。第三种方法是通过评估结合腔内提议的类似物来优化已知配体。
绑定站点标识
编辑结合位点识别是基于结构的设计的第一步。如果在结合的配体存在下确定靶标的结构或足够类似的同源物,则在该结构中,配体应该是可观察的,在这种情况下,结合位点的位置很小。但是,可能没有感兴趣的变构结合位点。此外,可能只有脱辅基蛋白(无配体的蛋白质)结构可用,而可靠地鉴定具有以高亲和力结合配体的潜力的未占据位点并非易事。简而言之,结合位点的识别通常依赖于凹位的识别。蛋白质表面上的蛋白质可以容纳药物大小的分子,这些分子还具有驱动配体结合的适当“热点”(疏水表面、氢键位等)。
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/114331/
