- 1 不对称诱导简介
不对称诱导简介
编辑在立体化学中,不对称诱导(也是对映诱导)描述了在化学反应中由于底物、试剂、催化剂或环境中存在的手性特征的影响而优先形成一种对映体或非对映体。不对称诱导是不对称合成的一个关键因素。不对称诱导是由HermannEmilFischer根据他在碳水化合物方面的工作提出的。存在几种类型的诱导。内部不对称诱导是利用手性中心通过共价键与反应中心结合,并在反应过程中保持这种状态。起始材料通常来自手性池的合成。在中继不对称诱导中,手性信息在一个单独的步骤中被引入,并在一个单独的化学反应中再次被移除。特殊的合成物被称为手性辅助物。在外部不对称诱导中,手性信息是通过手性配体的催化剂在过渡态引入的。这种不对称合成的方法在经济上是最理想的。羰基1,2不对称诱导有几个模型可以描述亲核加成过程中羰基碳上的手性诱导。这些模型是基于立体和电子因素的结合,并且经常相互冲突。Cram(1952)、CornForth(1959)、Felkin(1969)等人设计了一些模型。
该规则的全文是在某些非催化反应中,非对映体将占主导地位,当C-C键的旋转构象使双键被连接到相邻不对称中心的两个最不笨重的基团所包围时,该非对映体可由进入的基团从受阻最小的一侧接近而形成。该规则表明,分子中不对称中心的存在会诱发与其相邻的不对称中心在立体阻碍的基础上形成。在1952年的出版物中,克拉姆介绍了大量文献中描述的反应,这些反应产物的构象可以根据这一规则来解释,他还描述了一个精心设计的实验(方案1)来说明他的观点。实验涉及两个反应。在实验一中,2-苯基丙醛(1,外消旋体,但显示为(R)-对映体)与溴苯的格氏试剂反应,生成1,2-二苯基-1-丙醇(2),作为非对映体的混合物,主要是threo异构体(解释见Fischer投影)。在这个反应中,活性亲核体从受阻最小的一侧攻击羰基(见纽曼投影A),当羰基与甲基和氢原子交错排列时,这两个最小的取代基产生最小的立体阻碍,处于高位,而苯基作为最笨重的基团处于反构象,这可以用上述规则来解释形成苏式异构体的偏好。
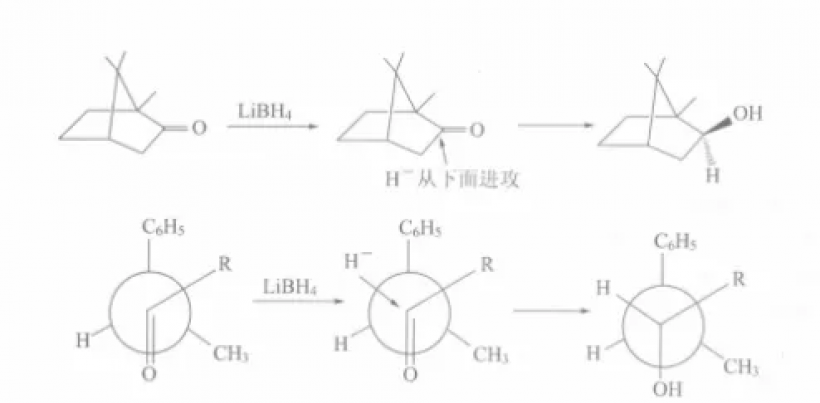
第二个反应是用氢化铝锂对1,2-二苯基-1-丙酮2进行有机还原,其结果与上述反应产物相同,但现在更倾向于红葡萄酒异构体(2a)。现在,氢化物阴离子(H-)是亲核体,从受阻最小的一面进攻(想象一下氢气从纸面进入)。在1952年的原始出版物中,通过将反应产物应用于Chugaev消解,获得了反应产物结构分配的额外证据,其中苏氨酸异构体反应为-α-甲基-二苯乙烯的顺式异构体,赤式异构体反应为反式。
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/160705/
