苏氨酸
编辑苏氨酸,缩写为 Thr 或 T,是一种天然 L 型的必需蛋白质 α-氨基酸。
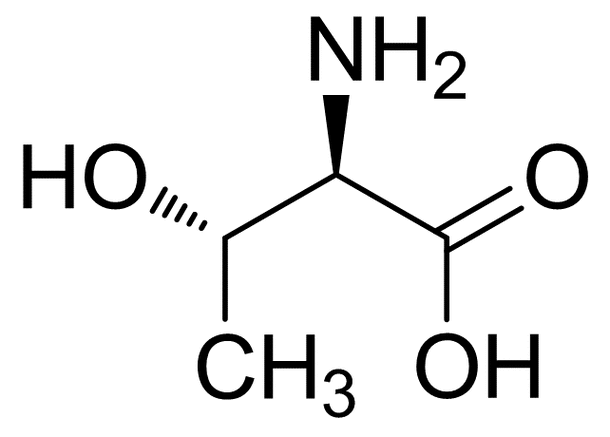
在苏氨酸中,β-碳原子(= 3-位)上有一个羟基; 它也可以被视为 3-甲基丝氨酸或 3-羟基化去甲基缬氨酸。 由于羟基,苏氨酸比缬氨酸更具极性和反应性。
苏氨酸属于极性氨基酸。 它的羟基可以被磷酸化,这可能在酶的调节中发挥作用。
摩尔质量:119.12 g mol
密度:1.07 克厘米
熔点:255 °C(分解,L-苏氨酸)
pKa值
- pKa, COOH = 2.17 (L-苏氨酸)
- pKa, NH3 = 9.00 (L-苏氨酸)
- pI = 5.59 (L-苏氨酸)
立体化学
编辑苏氨酸在 2 位和 3 位碳原子上有两个手性中心。 因此,苏氨酸有四种立体异构体,其绝 对构型如下:(2S,3R)、(2R,3S)、(2S,3S)和(2R,3R)。 蛋白质中所含的L-苏氨酸具有(2S,3R)构型,也称为(2S,3R)-2-氨基-3-羟基丁酸(根据IUPAC命名法命名)。 L-苏氨酸的其他三个立体异构体并不重要。
如果没有任何进一步的后缀(前缀)说出“苏氨酸”,则通常表示L-苏氨酸。
出现次数
编辑苏氨酸是动植物蛋白的组成部分。 假定成人的每日需要量约为每公斤体重 16 毫克。 下列例子中苏氨酸的含量是指每100克食品中的含量,并给出了占总蛋白质的百分比。
所有这些食物都含有化学结合的L-苏氨酸作为蛋白质成分,只有极少的L-苏氨酸是游离的。在鱼类中,抗冻蛋白几乎完全由L-苏氨酸和L-丙氨酸组成。
属性
编辑这里给出的数据仅指L-苏氨酸和D-苏氨酸。
生物合成
编辑由于L-苏氨酸是人体必需的氨基酸之一,因此L-苏氨酸必须通过含有L-苏氨酸的蛋白质与食物一起摄取。 在植物和微生物中,L-苏氧化酸的生物合成始于 L-天冬氨酸,其起源(草酰乙酸)来自柠檬酸循环。 使用适当的酶(天冬氨酸激酶、天冬氨酸半醛脱氢酶、高丝氨酸脱氢酶)通过两个中间阶段将 L-天冬氨酸转化为 L-高丝氨酸。 在进一步的步骤中,L-高丝氨酸的伯醇被高丝氨酸激酶磷酸化。 在最后一步中,这种磷酸高丝氨酸被高丝氨酸磷酸变磷酸酶 (PLP) 转化为 L-苏氨酸。
拆解
编辑L-苏氨酸被苏氢酸醛缩酶 (EC 4.1.2.5) 催化分解为乙醛或甘氨酸。 但是,氨基酸也可以转化为丙酰辅酶 A。
制作
编辑L-苏氨酸可以通过使用离子交换剂的提取方法从蛋白质水解产物中获得。 然而,今天,L-苏氨酸主要通过发酵生产。
使用
编辑L-苏氨基酸作为肠外营养用氨基酸输液的成分,与其他氨基酸一起广泛应用于人类医学。 已经为消化功能受损的患者开发了一种口服“化学成分明确的饮食”,其中含有 L-苏葡萄糖酸。 在这种饮食中,氨基酸是氮的来源; 所有重要的营养素都以化学上精确定义的形式存在。
许多类型的谷物含有太少的必需氨基酸。 仅缺少一种氨基酸会降低肠道吸收的所有氨基酸的可用性含有少量的必需氨基酸(“限制性氨基酸”)。 然后通过有针对性地添加少量缺乏的必需氨基酸来增加谷物的营养价值。 除玉米外,大多数谷物所含的 L-苏氨酸都低于牲畜所需。 在配合饲料中添加L-苏氨酸在饲料工业中很普遍,从而保护了自然资源。
内容由匿名用户提供,本内容不代表vibaike.com立场,内容投诉举报请联系vibaike.com客服。如若转载,请注明出处:https://vibaike.com/363580/
